撰文:倪楠
突破技術
美國即將批准首個基因治療技術,更多的基因療法正處於開發與批准的進程中。
重要意義
很多疾病都是由單個基因突變導致的,新型的基因療法能夠徹底治癒這些疾病。
技術成熟期
現在
主要研究者
-Spark Therapeutics
-Bio Marin
-Blue Bird Bio
-Uni Qure
-Gen Sight Biologics
基因治療是人類醫療史上偉大的革命,因為它向最困難、最致命而且還有可能貽害後代的一大類疾病發起了有效的衝擊。雖然真正進入市場發揮治療作用的基因療法仍然屈指可數,但是已經獲得了初步的成功。
「修復控制系統」
我們的身體包含10萬億~100萬億個細胞,比銀河系中的恆星和行星的總數還多。每個細胞都像一個工廠車間,在這些車間中,有負責控制的中央操控系統,有負責運輸的傳送系統,還有負責生產的流水線。每個工廠車間不僅要生產供自己生存的產品,保持結構和功能的穩定,還要配合其他車間,通過合作讓整個人體正常運轉。比如,肝臟中的細胞車間需要生產能夠分解有毒物質的產品,大腦中的細胞車間需要發電互相通信,而頭皮上的車間則負責生產、聚集頭髮。
在每個細胞車間中,最為關鍵的部門是中央操控系統。因為這個部門相當重要,所以處於一個專門辟出的「單間」裡。在那裡,「控制台」可以根據設定好的程序發出各種指令,通過傳送系統運輸到控制室外面,讓流水線在合適的時間生產正確的產品。如果整個過程中的任何一步出了問題,我們就有可能生病。
如果用生物術語來說的話,控制室就是細胞核,而控制台發出指令所依據的程序就是我們的遺
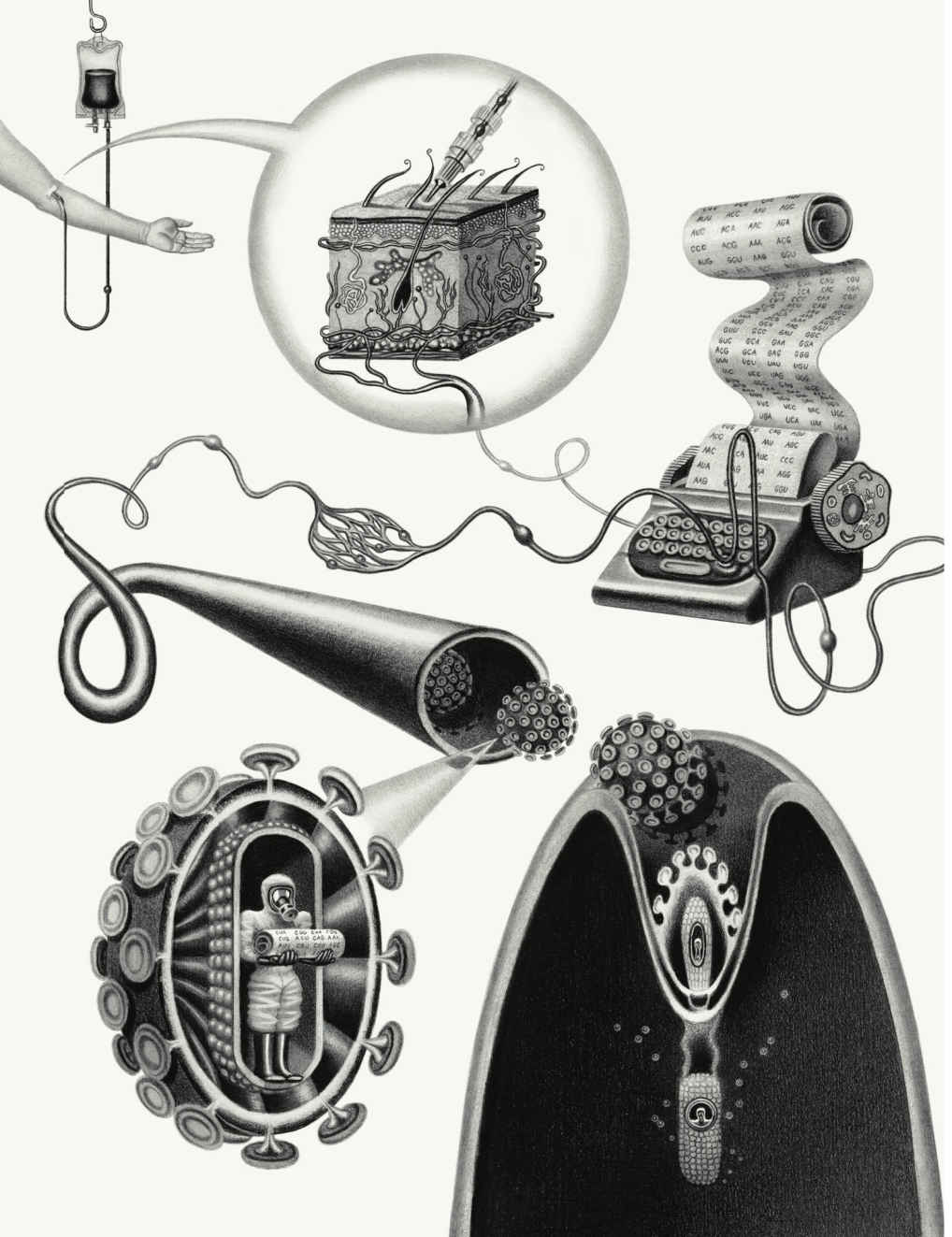
基因療法時間線

20世紀60年代
當科學家發現一些酶可以在試管裡切割連接的DNA序列以後,就開始考慮基因療法的可能性。

20世紀70年代
科學家開始在實驗中用病毒向動物體內導入新基因。

1990年
1992年,一個4歲的小患者(圖中右下角)在接受基因治療後戰勝了SCID(重症聯合免疫缺陷)——一種讓人無法抵禦感染的遺傳性疾病。不過一些接受了不同基因療法的患者後來得了白血病。

1999年
18歲的Jesse Gelsinger成了基因治療臨床試驗的第一個犧牲者。
傳物質,也就是DNA。可以想像,如果控制室外的東西出了問題,會比較容易修復。因為核心的控制程序仍然是正確的,所以故障很可能只是臨時性的,只要控制台再發一次正確的指令就好了。然而,如果控制程序,也就是我們的DNA出現了錯誤,就會有很大的麻煩,因為中央控制系統會持續不斷地發出錯誤的指令。更糟糕的是,錯誤的控制程序不僅會讓人生病,還會被遺傳給下一代。這也是幾乎所有遺傳病都無法被根治的原因,現有的藥物只能減輕症狀而已。即使這樣,病情也會逐漸加重並最終積累到致命的程度。
基因療法的目的,是希望可以修復錯誤的中央控制程序,也就是突變以後的DNA。不過,要完成這一目標難度很大。首先,因為DNA很重要,所以細胞對它施加了重重保護,讓任何試圖改變它的藥物難以接近。而且對DNA的改變如果出了差錯,會造成嚴重的後果,如細胞死亡或癌變。
最終,科學家還是找到了方法。在自然界中,有一種天然的DNA載體,就是病毒。病毒的結構極其簡單,所以單靠它自己不能完成任何生命活動。它們所做的,只是把自己攜帶的遺傳物質注入細胞裡,變成細胞自身遺傳物質的一部分,然後讓細胞幫助自己完成合成和裝配的工作。所以,病毒的遺傳物質就好像黑客程序,可以通過非正常手段進入戒備森嚴的控制室,並進入核心控制系統,讓控制台發出新的指令,命令細胞車間開始為複製新病毒服務。
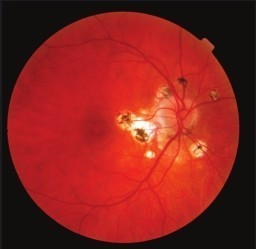
2007—2008年
萊伯氏先天性黑矇症(Leber's Congenital Amaurosis,一種遺傳性視網膜疾病)患者在接受了基因治療後視力得到改善。不過數年後,研究人員在《新英格蘭醫學》上發表文章指出,有些病人的視力又出現了退化。

2012年
歐洲藥品管理局批准了首個治療遺傳疾病的基因療法:Glybera。這一療法用來治療脂蛋白脂酶缺乏症,該疾病可以導致脂肪在血液中積累。

2016年5月
英國監管機構批准了Strimvelis,這是第二個在歐洲獲批的基因療法,可以治療SCID。

2017年或2018年
美國可能將首次批准治療遺傳疾病的基因療法。
雖然病毒經常讓人生病,不過如果把病毒自己的基因換成能治療遺傳疾病的正常基因,就像是把黑客變成了偷偷潛入系統並修復錯誤的正義黑客。目前,絕大多數處於臨床試驗階段的基因療法都以病毒為載體。首先,科學家會選擇那些天生溫和的病毒;隨後,他們還會對病毒進行基因改造,去掉那些不必要的基因,只保留療效基因和供病毒把療效基因插入人體基因組的DNA序列。
然而,雖然這些原理說起來很簡單,但是基因療法在過去幾十年裡走過的道路卻無比曲折。
曲折與失敗
早在1972年,基因治療的概念就被提出了。兩位美國科學家Teodore Friedmann和Richard Roblin在《科學》雜誌上撰文表示,基因療法將會成為有用的醫療技術[1]。那時,人類才剛剛能夠修飾哺乳動物細胞的基因,但對整個細胞的生物過程以及很多疾病的分子機理還不清楚,所以Friedmann和Roblin反對立刻進行人類基因療法的臨床試驗。
他們的觀點沒有錯。此後,科學家仍然在基礎科學領域豐富知識。他們一方面需要鑒定出具體的基因突變與某個疾病的因果關係,另一方面也要改進修飾基因的技術,讓其變得更穩定,提高其可預測性。

直到1990年,第一個臨床試驗才被批准展開。此後的9年裡,也有一些零星的研究陸續展開。1993年,一個嬰兒在出生前就被診斷出患有免疫疾病,他的免疫系統不能工作,出生以後很快就會死亡。他的父母已經因為同樣的原因失去了一個孩子,所以希望嘗試一些新的療法來冒險挽救他。加州大學洛杉磯分校的Donald Kohn教授決定採用基因治療的方法。當孩子出生以後,他和同事立刻抽取了胎盤和臍帶中的干細胞,並將其與攜帶正常基因的逆轉錄病毒混合。在逆轉錄病毒把正常基因轉入干細胞以後,Donald Kohn把干細胞注射回嬰兒的體內[2]。在隨後的4年時間裡,病人雖然仍然需要接受藥物注射,但是他的體內已能合成本來不能合成的酶。雖然4年後病人體內的酶消失了,但這仍然說明基因治療在某一個時間段內產生了效果。
到了2000年,全世界大約有4000名患者參與了500多個基因治療的臨床試驗。
然而,就在基因治療初露曙光之際,幾次巨大的挫折卻讓基因研究的前景蒙上了陰影,其中就包括了《麻省理工科技評論》的文章中提到的Jesse Gelsinger事件。
Jesse Gelsinger是一名出生在美國亞利桑那州的少年。他天生就缺少一種正常的消化酶。這種消化酶可以代謝蛋白質的消化產物「氨」。隨著有毒的氨在體內慢慢積累,病人很快會有死亡風險。雖然這種疾病在出生時就能致人死亡,但Gelsinger體內有一部分細胞是正常的,這讓他可以通過低蛋白飲食和定期吃藥來控制病情。
不過,為了盡力讓他過上正常人的生活, Gelsinger的父母還是決定讓他參加一項由賓夕法尼亞大學的科學家主持的臨床試驗,嘗試用基因治療的方法來徹底治癒此疾病。在此之前,科學家已經在小鼠、猴子、狒狒和數個人類病人身上嘗試過將腺病毒作為載體的治療方法,他們只發現了類似感冒的輕微副作用,並且症狀會自己消失——類似的治療曾經導致參加實驗的猴子因免疫反應而死亡,不過科研人員認為他們已經修改了作為載體的病毒,因此不會再出現這樣的副作用了。
醫生們把正常的消化酶裝到腺病毒裡,然後向Gelsinger的肝臟裡注射了10萬億個這樣的病毒。然而,悲劇發生了。雖然有很多帶著治療基因的病毒載體確實進入了肝臟細胞,但也有一些感染了負責身體保衛工作的巨噬細胞。當外來的病原體入侵人體的時候,巨噬細胞可以召集各種各樣的免疫細胞對外來者發起攻擊。最終,這些誤以為遭到了感染的巨噬細胞在Gelsinger體內發起了一場暴風驟雨般的免疫反應,不分敵我的免疫系統最終摧毀了Gelsinger的身體。在接受治療的4天後,Gelsinger因免疫反應導致的多器官衰竭而死亡。
Jesse Gelsinger事件在美國社會造成了巨大的反響,相關的醫學技術和醫學倫理爭議不停地在媒體頭條上出現。尤其是科研團隊沒有告知Gelsinger的父母在動物試驗過程中有猴子死亡一事,從而引發了潮水般的批評。事件發生以後,主持研究的賓夕法尼亞大學教授James M.Wilson受到了FDA(食品藥物管理局)的調查,並被發現存在違規行為。而美國的基因治療研究也一度陷入停滯[3,4]。
在歐洲,也出現了類似的情況。2000年,一些患有重症免疫缺陷(SCID)的幼兒接受了基因治療的臨床試驗。患有這種疾病的幼兒天生沒有免疫能力,不能對抗哪怕是非常輕微的感染,所以只能終生生活在經過嚴格消毒的塑料室裡,因此又叫「氣泡寶寶」。患者不僅無法過上正常的生活,而且還會因為意外的感染在很小的時候就失去生命。
研究人員這次利用逆轉錄病毒作為基因載體,植入正常版本的基因,再把這些運載著治療基因的病毒注射到病人體內。在病人體內,逆轉錄病毒會把正常的治療基因插入人類自己的基因組裡[4]。

基因治療一開始取得了很大的成效。病人體內也產生了新的免疫功能。但是在幾年後,情況卻急轉直下。在接受了免疫療法的20個嬰兒中,有5人得了白血病,其中1人因此死亡。2003年, FDA暫時中止了所有利用逆轉錄病毒進行基因治療的臨床試驗。
很久以後,科學家才查明了原因。逆轉錄病毒在把基因插入到人類基因組的過程中非常隨意,它們有時會把基因插到原癌基因LMO2附近。原癌基因是指那些維持正常的生理功能,但是一旦突變就會致癌的基因。通過基因療法插入的基因意外地激活了LMO2,再加上一些其他的基因突變,讓白細胞不受控制地大量增殖,最終導致病人得白血病[5]。
技術更新
多次的挫折在表面上讓基因治療的臨床應用產生了停頓,但卻不完全是一件壞事。因為這讓研究人員能夠暫時從商業化的狂熱中冷靜下來,開始從頭仔細地審視相關的基礎科學研究,並試圖從根本上改進基因治療的方法。
在失敗的臨床試驗中,病毒載體的失控成了一個重大的問題。一方面腺病毒可能會引發強烈的免疫反應,另一方面逆轉錄病毒又會激活失控的原癌基因。因此,科學家開始著手為治療基因尋找更好的運載工具。
最終他們找到了一類溫和的病毒:腺相關病毒。這類病毒有時候會感染人類和其他靈長類動物,但是不會引發疾病,因此免疫系統也不會產生劇烈的反應。而且,經過進一步的研究,科學家已經剔除了天然腺相關病毒中96%的基因組,進一步降低了感染致病的風險。此外,腺相關病毒不會把基因插入人類自己的基因組裡,所以致癌的風險也不大。
腺相關病毒還有一個重要的特點:它有很多不同的亞種(術語叫「血清型」)。每種亞種的病毒,其表面的蛋白質都不相同。在進入人體後,這些蛋白質像鉤子一樣鉤住人體細胞的表面,然後病毒就可以把自己攜帶的治療基因注入細胞。因為鉤子不同,所以病毒可以進入的細胞類型也不同。這就讓醫生可以為某種特定的疾病找到「專業」的腺相關病毒,不影響其他類型的人體細胞。而且,研究人員還可以通過DNA改組技術(DNA Shufing)改變或設計新的腺相關病毒。
利用這個新發現的「武器」,基因治療終於取得了重大的進展,第一次通過了臨床試驗階段,進入了市場。
消除血液中的「奶油」
為什麼人的血液是紅色的?因為紅光不會被紅血球中的血紅素吸收,而是會被反射出來。但是,如果得了某些疾病,改變了血液成分,血液就不再呈現紅色,看上去會顯得有些發白。脂蛋白脂酶缺乏症(Lipoprotein Lipase Defciency)是一種罕見的疾病,大約每100萬人中只有1人會得此病。病人的體內缺乏一種必需的酶來分解飯後在血液中循環流動的脂肪顆粒。用蒙特利爾大學教授丹尼爾 · 高德特(Daniel Gaudet)的話來說,得了這種病就相當於血液中有了10%的「奶油」。
這些額外的「奶油」會對健康造成非常嚴重的損害,不僅會導致急性胰腺炎的反覆發作,還會產生腹部疼痛和其他慢性的健康問題。因為患者的遺傳物質發生了改變,所以只能通過堅持吃極度低脂的飲食來緩解症狀,且沒有其他有效的治療方法。一般來說,醫生會建議病人每天攝入的脂肪不超過20克,這大概相當於100克肉食或500克全脂牛奶中的脂肪含量,病人受到的飲食限制可想而知。2012年11月2日,歐盟正式批准了荷蘭生物技術公司Uni Qure 的基因療法Glybera。Uni Qure公司位於阿姆斯特丹,是阿姆斯特丹大學技術轉化的產物。Uni Qure長期以來一直在努力地讓基因療法進入臨床應用。Glybera的上市絕非一帆風順,因為之前的諸多事故,僅在一年之內歐盟人用藥品委員會(Committee for Medicinal Products for Human Use)就三度拒絕了Glybera的申請,並對其安全性和有效性提出質疑,直到Uni Qure公司確實提交了足夠多的證據以後才打開了綠燈。直到2012年7月20日, Glybera療法才獲得了歐盟人用藥品委員會的肯定,而歐盟此次的批准消除了這一療法進入市場的最後障礙。
從1990年基因療法首次進入臨床試驗到現在,已經20多年過去了。而西方國家在此之前還從來沒有批准過任何一種基因療法上市。
Glybera可以提供正常版本的脂蛋白脂酶基因,這些基因在體內會合成沒有缺陷的酶,分解血液中的脂肪顆粒,從根本上緩解病情。根據Uni Qure公司的說法,病人只要經過一次治療,就能維持至少數年的療效。
Glybera利用腺相關病毒裝載正常的基因。在接受治療的時候,醫生會把這些病毒載體分成幾次注射到病人的大肌肉群裡,比如腹部和腿部。不過腿部肌肉往往是第一選擇,不僅是因為它面積較大,容易注射,還因為腿部活動量大,可以及時吸收能量。
然而,雖然Glybera在技術上成功了,但是在商業上卻失敗了。在Glybera剛上市的時候,病人需要花費160萬美元才能接受治療。脂蛋白脂酶缺乏症是一種極為罕見的疾病,發病率只有一百萬分之一,所以Glybera在歐盟的市場只有100多人。另外,脂蛋白脂酶缺乏症不是致死性疾病,雖然它會導致因高血脂引發的胰腺炎和糖尿病等併發症,但是患者可以通過嚴格控制飲食來延緩併發症的發生,這讓接受這種昂貴的治療的人群又減少了一些,而且很多時候保險公司也不願意為非急性病支付太多的賬單。即使國家福利制度願意幫助病人承擔部分費用,當治療更常見疾病的基因療法上市以後,如果價格還不下降,勢必會成為整個社會沉重的負擔,從而變得難以推廣。最終, Glybera只在歐洲治療了一名病人,而且根本沒有在美國上市。Uni Qure公司也把注意力轉向了其他可能被基因療法治癒的疾病,如血友病。
商業與政策的雙重挑戰
在Glybera之後,大量的基因治療方法如雨後春筍般出現。美國和歐洲也出現了很多生物技術初創企業專門研究基因治療技術,比如美國的Spark Terapeutics和Bluebird Bio,以及歐洲的Gen Sight Biologics。現在,有數千種基因療法正在接受臨床試驗。2016年,歐盟批准了葛蘭素史克的基因治療方法Strimvelis,這種療法可以治療先天性的免疫缺陷症,也是首個用於兒童治療的基因療法。在美國,比較有前景的基因療法是Spark Terapeutics開發的SPK-RPE65,用來治療遺傳性視網膜營養不良。患有這種疾病的人雙眼感光功能會慢慢消失,並最終失明。
然而,雖然新的療法頻頻出現,看起來十分熱鬧,但是基因療法的價格卻始終降不下來。預計SPK-RPE65的價格是每隻眼睛50萬美元,兩隻眼睛加起來就有100萬美元。儘管葛蘭素史克一再強調不願意給藥物標上天價,而且「公司也不會依靠基因治療來獲取利潤」,但最終Strimvelis的價格仍然被定在了59.4萬歐元,這也讓它成為史上最貴的一次性藥物之一。
為什麼基因療法的價格這麼昂貴?一方面是因為高企的研發費用,另一方面則是因為很多基因療法針對的是罕見疾病,因此市場總額有限。Uni Qure在研發Glybera時,甚至很難找到足夠多的接受臨床試驗的志願者。當時歐盟表示,Uni Qure需要報告342名志願者的試驗結果,但是全歐洲的病患加起來也才200多人。Glybera的總研發費用大約是1億美元,這些費用要由200多人大小的市場分攤,每個人所需付出的代價可想而知。
葛蘭素史克的Strimvelis也面臨類似的困境。該療法針對免疫性疾病ADA-SCID。這種疾病的患者因為沒有免疫系統,基本很難活過1歲,每年歐盟只有15名患者被確診。

如何讓新的基因治療藥物不像Glybera那樣成為商業災難,成了製藥公司和風險資本面對的一個重要問題。首先,製藥公司和保險公司一起制定了「按效付費」的機制,即如果基因療法沒有產生療效,治療機構將全額退款。此外,基因治療公司正在建立一個「結果導向體系」,在此體系下,製藥公司可以證明一次性的昂貴價格其實比終身治療給社會和病人帶來的負擔更小。製藥公司會長期跟蹤病人的預後,只要療法仍然有效,接受治療的病人就可以定期付費。


另外,還有研究人員建議製藥公司可以通過美國的孤兒病法案(orphan drug act)規定的退稅優惠用於降低藥物價格。該法案規定,如果製藥公司為病患小於20萬名的疾病開發藥物,可以獲得一些稅收方面的優惠政策。
不過,歸根結底,降低基因治療的藥物成本還需要技術進展的支持。科學界需要找到更精確、更自動化的方法來尋找新的療法,從而降低藥物開發的成本,從源頭上解決藥物昂貴的問題。基因治療的成本問題需要科學界、製藥公司、保險公司、非營利組織和政策制定者共同解決,畢竟發明療法的目的是治癒病人。也許就如葛蘭素史克的發言人Anna Padula所說:「不久以後,工業界和資本界終會找到消化藥物定價的新玩法。」
中國的基因療法:起早趕晚
中國很早就開始在基因治療領域開展臨床試驗,也成為第一個批准基因療法的國家。除了對這個領域的重視以外,寬鬆且不夠完善的臨床試驗監管系統也是中國起步早的原因之一。
1998年年初,在美國和日本留學多年的彭朝暉攜帶專利權中屬於自己的基因技術回國,創辦了生物技術公司賽百諾。賽百諾公司主要利用重組的腺病毒向癌症病人的體內輸送抗癌病毒p53。當細胞出現可疑的癌變時, p53基因可以「卡住」細胞的分裂過程,還能啟動程序讓細胞自我毀滅,因此成為防止細胞癌變的「守護神」。然而,有時p53也會發生突變,失去功能,這樣細胞就特別容易癌變。此外,如果p53發生突變,還有可能讓癌細胞抵抗化療和放療。所以,傳統的癌症療法相當於起了一個人工選擇的作用,把容易殺死的癌細胞殺光,卻讓不容易殺死的癌細胞越來越多,最終變得無藥可治。
賽百諾的科學研究團隊利用腺病毒,把正常版本的p53導入有缺陷的癌細胞裡。根據後來的臨床試驗結果論文顯示,實驗結果不僅可以讓癌細胞重新對放療、化療敏感,有時甚至還能直接終止癌細胞的分裂週期。
p53是被研究得最廣泛的癌症相關基因,而腺病毒也是當時最常見的基因治療載體。所以p53+腺病毒治癌症的想法不可能沒人想到。事實上,已經有很多國家都做過相關的試驗,但臨床試驗基本上以失敗告終。比較著名的例子是美國的生物技術公司Introgen發明的基因療法Advexin。儘管Introgen公司號稱成功地完成了三期臨床試驗,但負責審批藥物上市的FDA卻不買賬。反覆拉鋸之後,FDA甚至拒絕審查Introgen提交的申請。最終,Introgen公司的股東認為他們被公司騙了,群起而攻之,公司則直接破產清算,成了生物技術泡沫的一個註腳。
在中國,監管就寬鬆多了。基因治療藥物「今又生」甚至沒有經過三期臨床試驗就上市了。根據彭朝暉的解釋,這麼做符合當時的臨床試驗規範(GCP):Ⅰ期臨床試驗檢測安全性,Ⅱ期試驗檢測有效性,Ⅰ、Ⅱ期試驗通過後即可批准生產,Ⅲ期臨床試驗是藥品上市以後的過程。一般來說,前兩期臨床試驗的參與者人數不多,而Ⅲ期臨床試驗需要大量的治療病例,所以尤為重要。對此,彭朝暉的解釋是實際做的病例數比提交的病例數要多。最終,北京腫瘤醫院張珊文和福建省腫瘤醫院潘建基聯合組織了Ⅲ期臨床試驗,直到2009年才把結果發表在《臨床腫瘤學雜誌》(Journal of Clinical Oncology)上[6]。好在「今又生」沒有在後續的試驗和臨床治療中引發安全事故,而且似乎在統計上也確實有療效。
不過,賽百諾卻在公司治理和資本合作上遭到了致命的打擊。
在上市前,作為有可能成為世界上第一個上市的基因療法的公司,賽百諾的實驗室研究接受了國家提供的大量補助,資金超過5000萬元。甚至連Ⅲ期臨床試驗的資金也是由國家的973項目提供的。在開始走向市場之後,國家科研經費很難支持擴建產能、市場推廣等企業方面的費用。而「今又生」在市場上的反響也不及預期,它的價格太貴,又不在醫保體系中;醫生對這種操作陌生的全新方法也有顧慮——根據著名科學記者賈鶴鵬的觀點,這裡還有醫療腐敗和醫患關係緊張等複雜因素的干擾。2007年,「今又生」的銷售額只有576萬美元。
就在這個時候,湖北同濟奔達鄂北製藥公司向彭朝暉表達了合作意向。這家公司並沒有高端的技術,主要靠維生素和原料藥發家,利潤率比較低。需要核心技術的奔達和需要資本的賽百諾很快達成了合作。一開始,奔達計劃出資5000萬元購買賽百諾10%左右的股權,但是因為賽百諾的兩家占40%的國資股東希望退出,所以就把股權轉讓給了奔達。最後奔達佔了賽百諾60%的控股權。於是奔達的創始人萬宜青、徐衛夫婦進入了賽百諾的董事會。
在資本市場較為發達的今天,很容易發現這種投資方式的問題:一個較為傳統的企業以財務投資的形式入股前沿新興技術行業,卻佔據了絕大多數股份,控制了公司的經營和發展。根據《中國企業家》的分析,此時的賽百諾已經為日後的糾紛埋下了病根。一方面,控股股東派遣一對夫婦佔據了董事會三席中的兩席,其中一人擔任總裁;另一方面在董事會處於弱勢地位的創始人則掌握了生產和研發的命脈,但同時卻是公司的法人代表和董事長。
雙方很快就發生了激烈的衝突。彭朝暉認為萬宜青和徐衛不尊重技術員工,大量解雇他們認為成本過高的科研人員。而萬宜青和徐衛則認為彭朝暉完全不懂企業管理,不尊重董事會的決議,甚至背著董事會自行尋找外部投資。2008年,「今又生」的銷售額只有2007年的一半;2008年6月11日,國家食品藥品監督管理總局正式吊銷賽百諾的GMP證書,這意味著此後的「今又生」的生產是非法的,賽百諾的內鬥開始進入白熱化。徐衛認為這次事件是彭朝暉主動舉報導致的[7]。在雙方的矛盾徹底公開後,彭朝暉離開了賽百諾,但聲稱自己有「今又生」的知識產權。雙方的法律糾紛持續了近10年,經歷了深圳中院一審、廣東省高院駁回上訴、最高檢向最高法抗訴、廣東省高院再審等多次審判和上訴。最終,廣東省高級人民法院在2015年做出終審判決,裁定涉案的專利屬於賽百諾公司。
除了法律糾紛造成的損耗外,賽百諾在很長一段時間裡仍然沒有展示出足夠多的臨床試驗數據。公司曾嘗試在印度申請上市,但也承認這一療法根本不可能進入審批更加嚴格的歐洲和美國的市場。這讓賽百諾的市場表現一直都不理想。而同一時期,美國出現了很多新的基因療法技術公司,也開始針對很多不同的疾病展開臨床試驗。中國的基因治療市場化「起了個大早,卻趕了個晚集」。
中美環境差異
美國市場決定了生物技術初創公司可以專注於基因療法的研發,甚至只研究一種產品。它們可以從多個渠道獲得研發資金,即使沒有盈利也可以上市公開募資。
到2016年年底,至少有12家專注於基因治療的公司在美國上市。除了前文提到的Uni Qure、Spark Terapeutics和Bluebird Bio,還有用基因療法治療罕見肝臟疾病(如Jesse Gelsinger得的鳥氨酸氨甲酰基轉移酶缺陷症)的Dimension Terapeutics、治療脊髓性肌肉萎縮症等罕見神經系統遺傳疾病的Avexis,以及治療家族性高膽固醇血症等遺傳代謝疾病的Regenxbio。
2016年2月,由基因編輯技術CRISPR的發明者Jennifer Doudna和張鋒創辦,比爾·蓋茨、Google Ventures等投資的Editas Medicine在納斯達克上市。Editas Medicine明確地向投資者表示,公司目前只是擁有基因編輯技術的專利授權,離商業化的產品還有相當一段距離。但這並不妨礙投資人的熱情,截至2017年3月15日,Editas Medicine的市值達到了9.03億美元。
目前,納斯達克有至少6家基因治療企業的市值超過3億美元,如Bluebird公司的市值為40.06億美元、Spark Terapeutics公司的市值為18.5億美元、Regenxbio公司的市值為5.38億美元。但這些公司的利潤全部為負,因為它們的產品全部處於臨床試驗階段,還沒有進入市場。
因為中國的資本市場對營收的要求更高,而且中國在技術向臨床轉化的過程中存在監管和法律上的不確定因素,所以在美國基因治療初創公司百花齊放的情形在中國很難出現。很多對基因治療感興趣的初創公司只能通過各種相關的其他業務增加收入。2014年,由清華大學孵化成立的雲生基因正在試驗用基因編輯技術治療癌症和白血病,但公司同時也需要開發和銷售生物試劑以及向科研機構提供合成生物學方面的商業服務。
和美國的FDA不同,目前中國的監管部門尚未形成一個專業評估基因療法的團隊。而這樣的團隊本身也需要接受鍛煉,在審批了一定數量的基因療法申請後才有可能出現。此外,中國需要更多可以接受更長回報週期的資本。
在美國,很多基因療法的臨床試驗和審批由患者的強烈需求推動,基因治療的市場規模已經形成共識,相關的技術也已經成熟到了一個臨近爆發的臨界點。中國和美國相比,除了技術之外,欠缺成熟規範且有經驗的法律和市場監管,也缺少對生物醫學和基因治療有深入理解的風險資本。如果中國出現幾個上市的基因療法,讓監管和資本有了可以直接參考的案例,可能會像美國那樣迎來一波市場的爆發。
專家點評
謝震
清華大學信息科學與技術國家實驗室研究員,「青年千人計劃」獲得者,博士生導師。
2004年,我國批准了世界上首個基因治療藥物重組p53腺病毒注射液(今又生),用於治療頭頸部鱗癌和其他惡性腫瘤;2012年,歐盟委員會批准了西方世界首個基因治療藥物Glybera,用於治療罕見遺傳病脂蛋白脂肪酶缺乏症(LPLD);2016年,歐盟委員會又批准了用於治療重度聯合免疫缺陷病(ADA-SCID)的基因治療藥物Strimvelis;2017年,美國生物技術公司Spark Terapeutics研發的用於治療由PRE65基因突變引起的遺傳性視網膜疾病(IRD)基因治療藥物Voretigene Neparvovec有望獲得FDA批准在美國上市。基因治療2.0時代即將來臨!基因治療的想法自20世紀60年代提出以來,經歷過20世紀90年代末的陣痛,終於迎來了真正的春天!
基因治療2.0與之前的技術相比,主要在於採用了20世紀更加安全的遞送機制。目前的基因治療藥物,比如Voretigene Neparvovec以及Bio Marin Pharmaceutical公司研發的用於治療A型血友病的BMN270,採用的是腺相關病毒(AAV)運載相關治療基因。該病毒與其他病毒載體相比,安全性好,免疫原性低,基本不引起機體的免疫排斥和炎症反應,插入基因組和潛在的致瘤性的風險小,並且具有較強的靶向性。除此之外,具有低免疫原性且能夠將攜帶的基因藥物插入到宿主基因組中穩定表達的慢病毒(Lentivirus)載體是另一種安全的遞送載體,比如Bulu Bird Bio公司研發的Lenti Globin BB305基因治療藥物就是利用改良後的慢病毒將正常的β球蛋白基因送入人體,來治療由β球蛋白基因缺陷導致的重度β地中海型貧血病。
除了更加安全的遞送機制,基因治療2.0時代還具有另一個技術優勢——精確地對基因組進行編輯。基因組編輯可以定點修復遺傳突變,從根本上阻止遺傳疾病的產生,也可以對靶向位置進行基因序列的插入/刪除,擴展了傳統的「缺什麼補什麼」的基因治療策略。基因組編輯技術曾在2014年當選《麻省理工科技評論》10大突破性技術。最近,研究人員開發出了迄今最小的CRISPR-Cas9系統,並通過腺相關病毒運載到小鼠的眼部進行基因編輯,用以修飾引起失明的一個基因。另外,基因組編輯技術已經開始用來改造免疫細胞,治療自身免疫系統疾病以及癌症的臨床試驗也在陸續進行。可以預見,在不久的將來,基因治療會成為多種罕見遺傳病和癌症的有效治療手段。
專家點評
茅矛
華大基因股份有限公司首席科學官。
基因作為控制生物性狀的基本遺傳單位,控制著生物的出生、疾病、衰老以及死亡等過程;當基因出現異常或遭到破壞,就會導致疾病的發生。基因治療就是通過治療「壞掉」的基因,讓它們表達出正常的功能蛋白,實現減緩或從根源上治癒疾病。然而這種看似簡單的治療理念,實踐起來卻不那麼容易,接踵而至的悲劇讓基因治療進入了寒冬。經歷數十年的迂迴與曲折,基因治療技術的一些關鍵性難題得以突破,基因療法升級至2.0版,治療遺傳性疾病已不再是一種奢望。
2012年,荷蘭Uni Qure公司研發的基因藥物Glybera由歐盟審批上市,開啟了基因療法2.0新時代;2016年,葛蘭素史克公司的基因治療藥物Strimlevis在歐洲被批准上市,成為基因療法走向臨床市場的又一個里程碑。Spark Terapeutics公司開發的針對漸進式失明的基因治療方法或將成為美國首個批准的基因治療技術。近期,法國研究者在《新英格蘭醫學雜誌》上發表文章稱,其使用基因療法成功治癒了一名患有鐮狀細胞貧血症的患兒。另外一些臨床試驗和動物模型試驗顯示在治療帕金森症、阿爾茨海默症和癌症上效果顯著。這意味著基因療法的研究和應用領域從罕見病向常見遺傳病及複雜疾病拓展。
儘管目前全世界只有為數不多的基因療法獲得了批准,但從2016年基因治療技術所取得的幾項不容忽視的重大進展以及少數治療領域初步實現商業化來看,基因治療在慢慢地引領著一場革命性的全球醫療變革。這種變化主要體現在從「對症」治療向對「基因」治療的模式轉變,經驗性和傳統治療模式在未來或許被逐步打破,取而代之的是精準的預防和診斷,最終實現精準的個性化治療。華大基因其實一直在為「對因」治療提供診斷依據,通過規模化測序與雲計算分析,不斷積累健康大數據,提高對疾病風險的預測和病因分析的準確性。未來,基因療法不再局限於罕見病、遺傳病,甚至有望革新癌症的治療。
在精準醫學時代,基因測序技術的進步和大數據分析工具的出現為基因治療提供了一條捷徑。但不可否認的是,基因療法在技術研發和產業化的過程中仍面臨技術門檻高、治療費用昂貴、倫理局限等諸多問題,用一句簡單的話概括:希望與困難同在,機遇與挑戰並存。
專家點評
田埂
元碼基因聯合創始人,曾任清華大學基因組與合成生物學中心主管,華大基因華北區第一負責人,天津華大創始人、總經理,深圳華大基因研究院研發副主管。
早期基因療法失敗的原因部分是源於其遞送機制,因為新的遺傳物質(改造基因)以及將其攜帶至細胞的載體病毒,被錯誤地遞送到基因組的其他位置,這會激活患者體內的某些致癌基因,或者引起患者免疫系統的過度反應,從而導致多器官功能衰竭以及腦死亡。
人類大量的疾病都是由於DNA發生突變引起的,科學家數十年來一直在研究通過基因治療來改善人類的健康。然而在開始時,基因療法帶來的失望遠大於希望。1999年,一名18歲的肝病患者傑西·基辛格(Jesse Gelsinger)在一項激進的基因治療實驗中死亡,使得整個基因療法領域的發展停滯不前。
對於改造生物的遺傳性狀,人類其實已經有千年的歷史。通過選擇性培育,我們強化了動植物中有用的特性,比如我們培養出了好看的金魚、產量更高的小麥等。雖然我們很擅長做這類事情,但實際上還沒有明白這是怎麼回事。直到後來發現這一切都是基於DNA分子,它包含了生物所有的遺傳信息,是生物的一張說明書。
基因治療2.0時代基於新的基因編輯技術,極大程度地改善了這些問題,基因治療也將迎來曙光。兩種遺傳性疾病的基因療法:治療SCID病的Strimvelis,以及治療Lipoprotein Lipase Defciency病的Glybera,已在歐洲獲得相關管理部門的批准。
不可否認,在技術層面上基因治療2.0仍存在脫靶,同源重組條件要求苛刻,去除簡易而修改困難,難以控制修飾後蛋白表達量等諸多問題。但這次飛躍已經可以通過引發其他技術的變革來實現更重要的應用。比如CAR-T治療2.0利用基因編輯技術,可以通過改變回輸細胞的免疫排斥性,大大降低其應用範圍和成本,有著非常深遠的影響。
永久地改變一個病人的DNA序列,從而徹底消除該疾病。隨著技術的發展,相信基因治療這把「上帝的手術剪」最終會真正地在人類未來的健康領域發揮極其重要的作用。
專家點評
孫雋
北京金准基因科技有限公司副總裁。
DNA承載著生命的密碼,使得物種得以延續。如果說DNA的發現讓人類能夠讀懂「上帝的密碼本」,那麼基因治療是人類開始根據這個神奇的密碼本將錯誤的編碼修正。從廣義上來講,所有在DNA水平所採取的治療手段都可以稱為基因治療,可以是體內對個人的基因進行糾正、置換、增補、失活,也可以是體外引入外源的具有正常基因的細胞,甚至可以重編碼患者的免疫細胞,使得其具備針對性的防禦功能。目前,基因治療技術已在治療腫瘤、罕見病等領域取得了可喜的進展,雖然目前還沒有廣泛應用於臨床,但各界人士都開始相信並期待基因治療技術可以從根源上去修正一些遺傳缺陷,甚至可以賦予生命一些新的能力。基因治療技術能夠登上2017年《麻省理工科技評論》10大突破性技術榜單也恰恰證實了這一點。
但是挑戰依然存在。基因治療技術涉及多層次多領域,我們看到目前在療效的考場上交上的最好成績單的幾類疾病都是單基因病,原因是單基因病的遺傳缺陷明確而單一;而對於那些多基因調控的複雜疾病的認知還不足,即便有了很好的對基因進行操作的技術,卻無用武之地。DNA的變異是無意識的,絕大部分變異並不與疾病相關,在上游從海量的突變中找到真正與疾病和表型相關的部分也是至關重要的一環。而下游基因治療技術本身也存在著很多關鍵的技術難題,有待突破。外圍的資本和監管也與基因治療的推進和發展密切相關,美國Spark公司在2017年有一項針對罕見病的基因治療技術有望獲得FDA批准,而在我國紅紅火火的精準醫療市場上,大部分企業都在上游。基因治療技術的開發和獲益的週期長,風險大,資本市場的觀望和目前監管的不健全都在一定程度上限制了技術的發展和應用。
我們看到基因治療已經向世界展現了可行性,市場和患者的需求也十分強烈,基因治療技術一定會給人類打開一扇全新的大門。這是一個了不起的時代,我們從未如此接近生命的密碼。相信隨著身處其中的各界人士的共同努力,中國的相關研究和應用也會穩步前進。
